硅烷偶联剂修饰的锂离子电池硅负极材料
二次电池现已被广泛应用于便携式消费电子设备,且目前也已逐步开始应用于电动汽车方向。它们同样也被认定为非常具有吸引力的储能设备[1-2]。锂离子电池(LIBs)因具有高的能量密度、良好的循环寿命以及高的动力性能获得了备受瞩目[3-4]。现有的锂离子电池多是采用石墨作为负极,LiCoO2、LiMnO4、LiFePO4[2]等金属氧化物或磷酸盐作为正极。而这些材料相对较低的比容量(石墨的理论比容量370mAh/g,金属氧化物/磷酸盐的理论比容量约为140 ~ 170mAh/g)限制了整个电池的应用[5]。
为了提高锂离子电池的容量,目前的科研工作人员一直致力于探寻高比容量的电极材料。在正极方向,硫化物[6-7]被广泛研究;而在负极方向,合金材料很有前景。理想的负极材料应具有高的质量比容量和体积比容量,低的脱嵌锂电位,长的循环寿命,良好的环境兼容性,低毒性以及低成本[8]。基于上述考虑,硅成为了最有潜力的负极材料。与其它的合金材料相比,硅有着最高的质量比容量(4200mAh/g,Li4.4Si)和最高的体积比容量(9786mAh/cm3);除此之外,它还有着相对较低的嵌锂电位(0.4V vs Li+/Li)[9];硅同样还是地壳中第二丰富的元素。
然而,硅负极材料的容量保持率较低,容量衰减迅速[10-11]。这主要是因为其在脱嵌锂过程中有着很大的体积变化(体积膨胀率高达420%),从而导致材料粉化进一步可能从集流体上脱落,同时会伴随着不断有新的SEI膜的生成。
硅烷偶联剂多用于表面处理,借以提高材料的机械性能、耐候性、耐水性、粘结性、分散性等。本文借助硅烷偶联剂的交联作用在硅负极材料表面形成一层有机薄膜,从而改善硅负极的循环稳定性。硅烷偶联剂的通式为Y-Si-X3,其中Y表示疏水基,如环氧基、巯基、乙烯基等;X表示可水解基团,可水解或醇解为羟基,从而变为硅醇,如酰氧基、氯基、烷氧基、氨基等;下图表示为偶联剂与硅的作用机理:
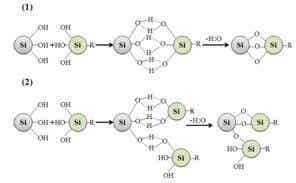
图1 硅烷偶联剂与硅的作用机理[12]
通过耦联反应在纳米硅表面包覆一层有机薄膜,这层薄膜不仅可以起到缓冲硅体积膨胀的功能;同时可以对硅表面进行处理,使其由亲水性转变为疏水性,减少其团聚度,同样也可以提高其在有机电解液中的分散性。
本文主要采用γ-缩水甘油醚氧丙基三甲氧基硅烷(KH560)对纳米硅粉进行改性处理,来提高硅负极材料的循环稳定性。
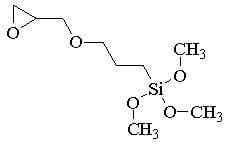
图2 KH560的结构式
2 实验
2.1 改性纳米硅的制备
提前将一定量的KH560用18mL的无水乙醇和2mL pH为4.0的草酸溶液水解12 h。
将1.0 g的纳米硅粉(商业用)分散至盛有无水乙醇和蒸馏水(体积比为9:1)混合溶剂的三口烧瓶中,超声分散0.5h。将烧瓶置于油浴锅内,磁力搅拌,在氮气保护条件下,升温至90℃后加入已水解的KH560。回流条件下,反应5 h。待温度冷却至室温后,使用无水乙醇离心洗涤2 ~ 3次。而后将离心产物120℃真空干燥10 h,即可得到改性纳米硅,记为KH560-Si。例,当以质量分数为5%的偶联剂进行修饰时,即可记为5%-KH560-Si。
2.2 电池的制备
采用水性膏和膏的方法制备极片,铜箔为集流体。电极材料、粘结剂、导电剂的质量比为80:10:10。其中,粘结剂采用羧甲基纤维素钠(Carboxymethylcellulose sodium,CMC)、导电剂采用导电炭黑(Super P)。
和膏时,先称取一定量的CMC溶解于蒸馏水中,磁力搅拌,直到其完全溶解之后,加入导电剂Super P,搅拌均匀后,加入电极材料,继续磁力搅拌约6 ~ 8 h。用涂布器将其均匀涂布在集流体上,80℃条件下,真空干燥8 ~ 10 h。冷却至50℃以下后,将其从烘箱中取出,冲切成半径为7 mm的圆片,称重、记录,而后继续80℃真空干燥8 ~ 10 h。
冷却至室温后,移入手套箱,以锂片为负极,聚丙烯薄膜为隔膜,电解液采用体积比为1:1:1的EC/DEC/EMC+1mol/L LiPF6,组装成CR2025型的扣式电池。从手套箱中取出后,用封口机封口,静置8~10h后再进行电化学性能测试。
2.3 电池的测试
用Nicolet公司生产的Avatar 360 型红外测试仪对改性材料进行了红外光谱分析。用日本日立公司生产的S-8020型的扫描电子显微镜对改性材料的微观形态进行了形貌观察。用Neware BTS-9000电池检测系统对电池进行了恒电流充放电测试,放电(嵌锂)终止电压为0.01V,充电(脱锂)终止电压为1.5V,其中恒定电流值的设定参考电流密度为100 mAh/g。
3 结果与讨论
3.1纳米硅的扫描电子显微镜测试分析
对商业纳米硅粉进行了扫描电子显微镜形貌观察。由图3-A可以看出,纳米级的硅颗粒呈球状,且团聚现象十分严重;而由图3-B可以计算出该纳米硅的半径大约在30nm左右。本文主要通过对其进行改性处理,进而考察改性效果。

图3 纳米硅颗粒的扫描电子显微镜图
3.2纳米硅表面羟基数量的测定
将0.2g纳米硅用75ml质量浓度为20%的氯化钠溶液和25ml乙醇溶液溶解;密封条件下,搅拌处理5h;而后用0.1mol/L的盐酸将溶液的pH调至4.0,再用0.1mol/L的NaOH溶液将其pH调至9.0;根据式(1)来确定表面羟基的数量[13]:
(1)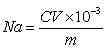
其中,C——NaOH溶液的浓度:0.1 mol/L;
V——pH值从4.0升至9.0时所消耗的NaOH溶液体积:ml;
m——纳米硅粉的质量:g。
经测定,最终所消耗的NaOH的量为0.32 ml。经计算可得出纳米硅粉表面羟基的数量约为1.6×10-4mol/g。这与文献中所介绍的数量级相符,表明该商业用纳米硅粉可以用来与KH560发生反应,进而形成一层有机薄膜,借以缓冲其在脱嵌锂过程中的体积膨胀与收缩。
3.3热重分析测试(TG)
对以质量分数为20%的KH560改性后的纳米硅进行了热重分析,其结果如图4所示:
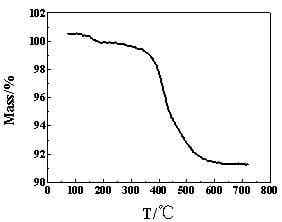
图4 20%-KH560-Si的热重
从图中可以看出,在低于200℃的温度下,有约为0.6%的重量损失,其对应为化学吸附和物理吸附水分的蒸发。在300~650℃的温度范围内,存在约为8.0%的重量损失,对应着有机硅烷的分解。根据式(2)可以计算出接枝率:
(2)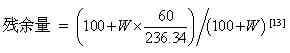
经计算可得接枝率为12%。当加入偶联剂的量为纳米硅质量的20%时,其嫁接上的量为12%左右。可能原因:纳米硅表面多个羟基与一个偶联剂分子发生了交联反应;偶联剂分子自身发生了交联反应,致使其嫁接在纳米硅上的量有所下降。
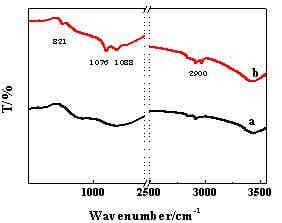
图5 FTIR测试:a:nano-Si;b:10%-KH560-Si
如上图所示,改性处理后的硅粉在821cm-1处出现吸收峰,其对应着为Si-C键的伸缩振动;1076cm-1出现Si-O-Si键的伸缩振动峰;1088cm-1处的峰则对应为Si-O-C的反对称振动峰;而2900cm-1处,表示C-H键的伸缩振动。分析表明,硅烷偶联剂KH560已嫁接在了纳米硅的表面。而就其没有明显的环氧键的峰,其原因主要在于,在酸性条件下,环氧基发生开环反应,生成了羟基。这同样也可以作为KH560的一个优势来考虑,即其相较于其它偶联剂而言,在水解过程中,会产生更多的羟基以便更均匀地嫁接在纳米硅的表面。

图6 纳米硅改性前后TEM图:A)改性前B)、C)10%KH560改性后
由上述图6-A可以看出其测试结果与SEM结果相一致,即本实验采用的纳米硅的半径约为30nm。同样可见,未经修饰的纳米硅颗粒具有光滑的边缘。由图6-B可以看出,改性的纳米硅,其表面变的粗糙,表明其表面已修饰上偶联剂KH560。经初步估算其半径约为35nm左右,故其包覆的膜厚约为5nm左右。但由图6-C可以看出,包覆的膜层其厚度并不均匀,故5nm仅仅可以看做一个平均值。
3.6循环性能测试结果分析
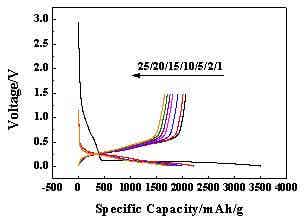
图7 10%-KH560-Si的充放电曲线
如图7所示,当以质量分数为10%的KH560进行改性处理后,其在循环至第10圈时,容量保持率为87.8%;循环至第20圈时,容量保持率为83.2%;循环至25圈时,容量保持率还剩80.7%。相较于纳米硅而言,这有很大的提升。
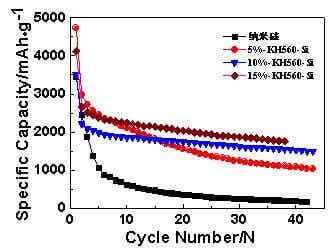
图8 KH560改性前后的循环性能对比图
由图8可知,在纳米硅表面嫁接上KH560后,能有效提升其循环性能;当偶联剂的浓度逐渐上升时,其循环性能也相对提高。这主要归功于偶联剂通过共价键合作用在纳米硅表面形成了一层有机膜,从而对其体积的膨胀与收缩起到了很好的缓冲作用,抑制了硅颗粒的粉化,同时也阻止了其与集流体的脱离。但偶联剂的浓度会决定膜的厚度与完整性,故随着偶联剂浓度的增加,其循环性能会有更好地提升。探寻其最佳修饰浓度将是我们的下一步工作方向。
4 结论
本文主要采用硅烷偶联剂KH560,通过简单的回流处理方法,在硅负极材料表面形成了一层有机包覆膜。该膜能对硅粒子的膨胀与收缩起到明显的缓冲作用,从而得到了循环性能良好的锂离子电池用负极材料。该方法同样适用于那些在脱嵌锂过程中存在体积膨胀的其它活性材料。
参考文献:
[1]Whittingham M S. Lithium batteries and cathode materials[J]. Chemical reviews, 2004, 104(10): 4271-4302.
[2] Liu C, Li F, Ma L P, et al. Advanced materials for energy storage[J]. Advanced Materials, 2010, 22(8): E28-E62.
[3] Scrosati B, Garche J. Lithium batteries: Status, prospects and future[J]. Journal of Power Sources, 2010, 195(9): 2419-2430.
[4] Yang Y, Jeong S, Hu L, et al. Transparent lithium-ion batteries[J]. Proceedings of the National Academy of Sciences, 2011, 108(32): 13013-13018.
[5]Armand M, Tarascon J M. Building better batteries[J]. Nature, 2008, 451(7179): 652-657.
[6]Yang Y, McDowell M T, Jackson A, et al. New nanostructured Li2S/silicon rechargeable battery with high specific energy[J]. Nano letters, 2010, 10(4): 1486-1491.
[7]Ellis B L, Lee K T, Nazar L F. Positive electrode materials for Li-ion and Li-batteries†[J]. Chemistry of Materials, 2010, 22(3): 691-714.
[8]Szczech J R, Jin S. Nanostructured silicon for high capacity lithium battery anodes[J]. Energy & Environmental Science, 2011, 4(1): 56-72.
[9]Huggins R A. Lithium alloy negative electrodes[J]. Journal of Power Sources, 1999, 81: 13-19.
[10]马增胜, 周益春, 刘军, 等. 锂离子电池硅负极材料衰退机理的研究进展[J]. 力学进展, 2013, 43(6): 581-599.
[11]Zhang X W, Patil P K, Wang C, et al. Electrochemical performance of lithium ion battery, nano-silicon-based, disordered carbon composite anodes with different microstructures[J]. Journal of power sources, 2004, 125(2): 206-213.
[12]陈思源. 锂离子电池硅基负极材料的改性研究[D]. 哈尔滨工业大学, 2014.
[13]刘立柱, 马红杰, 朱兴松, 等. 纳米 SiO2表面改性研究[J]. 化工新型材料, 2008, 35(11): 60-61.
作者简介:马刊 哈尔滨工业大学化工学院 研究生二年级
联系电话:18845075330
高云智 哈尔滨工业大学化工学院 教授/博导
联系电话:13614512363
联系地址:黑龙江省哈尔滨市南岗区西大直街92号(哈尔滨工业大学)
邮编: 150001
(马刊 高云智 )
(哈尔滨工业大学 化工学院)


